化学反応式の係数は、化学の世界で非常に重要な役割を果たします。私たちは、これらの係数が反応のバランスを保ち、物質の変化を理解する鍵であることを知っています。化学反応式の係数を理解することで、反応の進行や生成物の量を正確に予測できるようになります。
化学反応式 係数とは
化学反応式の係数は、反応の物質の量を示す重要な要素です。この係数は、反応式のバランスを保ち、反応の正確な進行を理解する手助けになります。以下に、化学反応式の係数を理解するためのステップを示します。
- 反応式を確認する。 反応する物質を特定し、生成物を明確に記載します。
- 各物質のモル数を考える。 反応における物質の量をモル数で把握します。
- 係数の役割を認識する。 係数が物質間の比率を示し、反応バランスを保つことを理解します。
- 反応の結果を予測する。 係数を基に、生成物の量を計算します。
- 反応の調整を行う。 必要に応じて係数を変更し、化学反応式が正しいか確認します。
化学反応式の基本
化学反応式は、化学反応の過程を表現する重要なツールです。係数を理解することが反応のバランスを取るために不可欠です。具体的には、次の内容を深堀りします。
反応物と生成物
反応物は、化学反応の開始時に存在する物質です。一方、生成物は反応後に生じる新しい物質です。この関係を把握することで、反応がどのように進行するかが理解できるようになります。つまり、次のポイントを確認します。
- 反応物を特定する。反応に関与する物質の名前や化学式をリストアップします。
- 生成物を特定する。反応後に得られる物質の名前や化学式も同様にリストアップします。
- 両者の関係を明確にする。どの反応物がどの生成物に変わるのかを理解します。
このプロセスを経て、反応の全体像が分かるようになります。
反応式のバランス
反応式のバランスは、化学反応が正確に記述されているかを示します。反応を表す際、質量保存の法則に従う必要があります。以下のステップでバランスを取ります。
- 反応物と生成物の元素をリスト化する。各物質に含まれる元素を列挙します。
- 各元素の原子数をカウントする。反応物と生成物で原子数を比較します。
- 係数を調整する。不均衡な元素の原子数を一致させるために、適切な係数を追加します。
係数の役割
係数は化学反応式において重要な役割を果たします。化学反応のバランスを確保し、物質の変化を理解する助けとなります。具体的には、係数が反応物や生成物の量の比率を明確に示します。
量の比率
量の比率は、反応物と生成物の関係を示す重大な要素です。以下のステップで理解を深めます。
- 反応物と生成物を識別する。化学式を見て、反応に必要な物質を特定します。
- 原子の数を数える。各元素の原子数をカウントして、どれだけ反応に関与するか確認します。
- 係数を設定する。質量保存の法則に基づき、反応物と生成物の比率を設定します。
- 反応式をバランスさせる。必要に応じて係数を調整して反応式の両側が均等になるようにします。
このプロセスを通じて、反応物と生成物の比率を正確に把握できるようになります。
化学反応の理解
化学反応を理解するには、係数の役割を把握することが不可欠です。なぜなら、係数が反応全体の進行を決定するからです。以下のポイントに注目して説明します。
- 反応の進行を予測する。係数によって生成物の量が明示されます。
- 化学反応の速さを示す。反応物の量により、速度が変化します。
- 反応の条件を把握する。温度や圧力によっても係数の影響が見られます。
係数の計算方法
係数の計算は、化学反応式のバランスを取るために欠かせないプロセスです。以下に示すステップを順に実行して、正しい係数を導き出しましょう。
係数を求めるステップ
- 反応物と生成物を特定する。 反応の参加者となる物質を理解し、正確に書き出します。
- 元素をリスト化する。 反応式に含まれるすべての元素を明示的に書き出します。
- 元素ごとに原子数をカウントする。 各元素の原子数を数えて、整理します。
- 初期の係数を設定する。 すべての反応物と生成物に対して初めの係数を与えます。
- 質量保存の法則に従って調整する。 反応物と生成物の原子数を一致させるため、係数を調整します。
- 全ての元素の原子数を確認する。 調整後、全ての元素がバランスを保っているか再チェックします。
- 最終的な係数を確定する。 すべての要素が整ったら、最終的な係数を明記します。
例題の紹介
次に、具体的な例を用いて係数の求め方を示します。以下の反応式を考えましょう。
C3H8 + O2 → CO2 + H2O
この反応の係数を求める手順を見ていきます。
- 反応物と生成物の特定:反応物はC3H8とO2、生成物はCO2とH2Oです。
- 元素のリスト化:C(炭素)、H(水素)、O(酸素)の3つの元素をリスト化します。
- 原子数のカウント:Cは3、Hは8、Oは2をカウントします。
- 初期の係数設定:各物質に対して初期の係数を1とします。
- 調整:質量保存を考慮し、最初に最も複雑な生成物であるCO2から係数を設定します。
- 確認:CO2を3、H2Oを4と設定します。この時点でOの原子数は6(3×2 + 4×1)になりますので、O2にかける係数も調整します。
- 確定:最終的な係数は、以下のようになります。
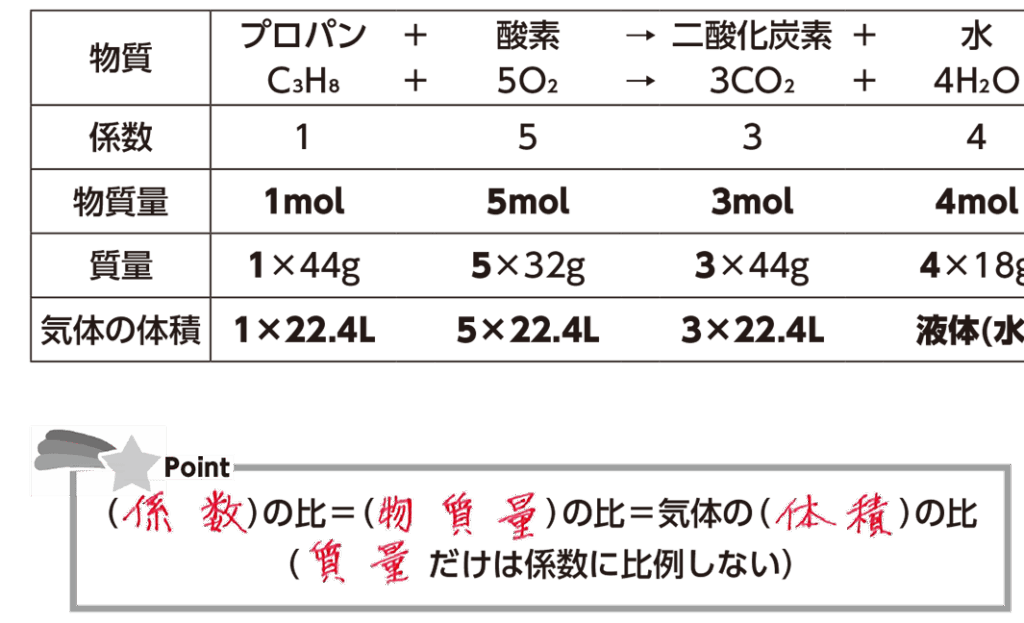
C3H8 + 5O2 → 3CO2 + 4H2O
係数と反応の種類
係数は化学反応式において重要です。反応の種類によって、係数の意味やその設定方法が変わります。ここでは、主な反応の種類について詳しく見ていきます。
硬化反応
硬化反応は、物質が固体に変化する過程です。この反応では、通常、以下の手順を踏みます。
- 反応物を準備する。必要な化学物質をすべて揃えましょう。
- 温度を調整する。硬化を促進するための適切な温度に設定します。
- 混合する。反応物を均一に混ぜ、化学反応が開始される準備をします。
- 硬化を観察する。時間の経過とともに変化を確認し、完成を待ちます。
この過程における係数は、各物質の比率を示し、反応の効率を決定します。
中和反応
中和反応は、酸と塩基が反応して中性物質を生成する方法です。この反応の実施には、次のステップが含まれます。
- 酸と塩基を選ぶ。適切な酸と塩基の組み合わせを選択します。
- 希釈する。酸や塩基を目的の濃度に希釈します。
- 滴下する。一方を他方に滴下し、反応の進行を観察します。
- pHを測定する。反応後の液体のpHを測定し、中和が成功したか確認します。
Conclusion
化学反応式の係数を理解することは私たちの化学的知識を深めるために欠かせません。反応物と生成物の比率を正確に把握することで反応の進行を予測しやすくなります。質量保存の法則に従ったバランスの取り方を学ぶことでさまざまな反応のメカニズムを明確に理解できます。
さらに異なる反応の種類によって係数の設定方法が変わることも重要です。これにより化学反応の効率や条件を把握しやすくなり私たちの実験や研究に役立ちます。係数の役割をしっかりと理解し実践することで化学の世界をより深く探求できるでしょう。